Bohr Atom Teorisi ve Modern Atom Teorisi 9. Sınıf Kimya
Aradığın Sınav veya Test Yok mu?
Yapay zeka ile TYT, AYT, KPSS ve okul derslerine özel online testler, konu özetleri ve PDF etkinlikleri saniyeler içinde hazırlansın. Tamamen ücretsiz!
BOHR ATOM MODELİ
Alevin üzerine bir tutam yemek tuzu döküldüğünde, alev rengi sarıya döner. Havai fişeklerin farklı renklerde patlamasının sebebi de budur. Yağmur yağdıktan sonra güneş çıktığında gökkuşağının oluşmasının nedeni de aynıdır.
Bütün bu olayların nedeni, spektrumlar ile ilgilidir.

Alev renginin sarı olması ve havai fişeklerden oluşan renkli ışıkların nedeni, farklı elementlerin ısıtıldığında farklı enerjili ışımalar yapmasıdır.
Beyaz ışık bir prizmadan geçirildiğinde, kendini oluşturan farklı enerjili ışınlara ayrılır. Bu yapıya spektrum (renk yelpazesi) adı verilir. Gökkuşağı olayında da damlacıklar prizma görevi yapar.
Beyaz ışıktan elde edilen, kırmızıdan mora tüm renkleri içeren spektrum sürekli (kesiksiz) spektrum olarak adlandırılır.
- Bir maddenin ısı enerjisi alması, absorpsiyon (soğurma), aldığı enerjiyi ışık şeklinde geri yayması ise emisiyon (yayma) olarak adlandırılır.
- Farklı elementlerin atomları, enerji alarak uyarıldıklarında, fazla enerjilerinin bir kısmını dışarıya yayarlar. Bu sırada her element için kendine özgü bir çizgi spektrumu oluşur.
Çizgi spektrumları, maddeler için ayırt edicidir. Bir maddenin emisiyon ve absorpsiyon spektrumlarındaki dalga boyları aynıdır.
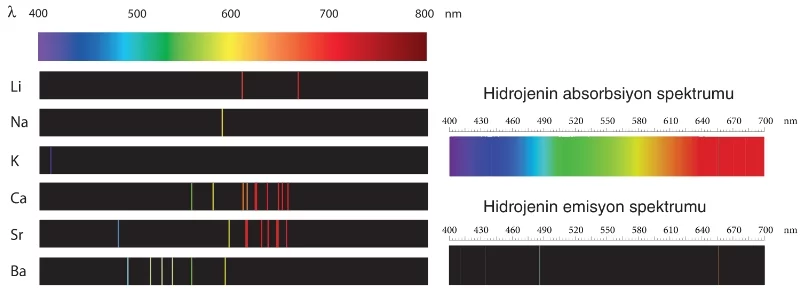
Niels Bohr, hidrojen spektrumunu inceleyerek yeni bir atom modeli ortaya atmıştır.
Bohr Atom Modeli’nin Varsayımları
- Atomda elektronlar çekirdek etrafında belirli yörüngeler üzerinde bulunur. Her yörüngenin belirli bir enerjisi vardır.
- Elektron, çekirdekten uzaklaştıkça sahip olduğu enerji artar.
- Elektronlar, kendilerine en yakın yörüngelerde enerji seviyesini kaybetmeden bulunabilir.
Bu yörüngeler merkezden itibaren K, L, M, N, O, … gibi harflerle ya da 1, 2, 3, … gibi sayılarla gösterilir.
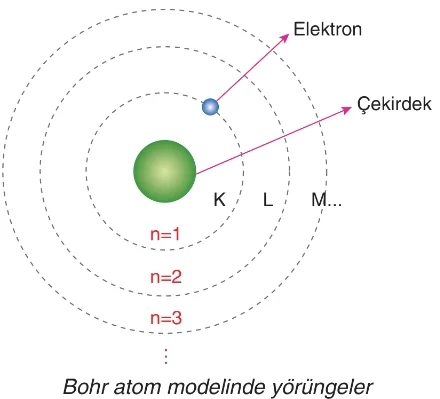
Çekirdeğe en yakın olan yörüngenin enerjisi en düşük olup, çekirdekten uzaklaştıkça yörüngelerin enerjisi artar.
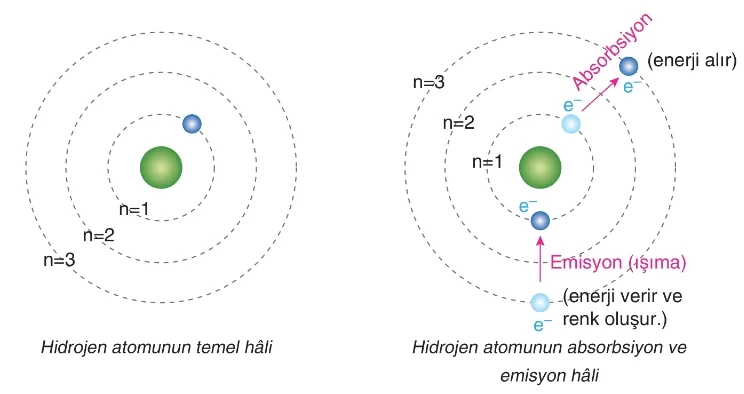
- Elektronun çekirdeğe en yakın, en düşük enerjili ve kararlı hâline temel hâl denir.
- Elektron, dışarıdan enerji alarak daha yüksek enerji düzeyine geçtiğinde, bu durum uyarılma olarak adlandırılır ve elektronun bu hâline uyarılmış hâl denir.
- Uyarılmış hâlde olan elektron, kararsızdır ve dışarıya enerji yayarak tekrar temel hâline dönebilir.
Bohr Atom Modelindeki Eksiklikler / Hatalar
- Bohr Atom Modeli, hidrojen atomu ile tek elektronu olan He⁺, Li²⁺ gibi iyonların spektrumlarını açıklayabilmiştir. Ancak çok elektronlu taneciklerin spektrumlarını açıklayamamıştır.
- Elektronların yörüngedeki hareketlerini tam olarak açıklamakta yetersiz kalmıştır.
- Elektronlar çekirdeğe çok yakın bir noktadan belirli yörüngelerle döndüğü için, bu model daha sonradan yetersiz bulunmuştur.
Bohr atom modelinin eksikliklerini gidermek için modern atom teorisi geliştirilmiştir. Modern atom teorisine göre, elektronların bulunma olasılığının yüksek olduğu bölgeler vardır. Bu bölgeler, belirli bir yörünge olarak değil, uzayda dağılan bir bulut şeklinde tanımlanır. Bu nedenle, modern atom teorisi bulut modeli olarak da bilinir.
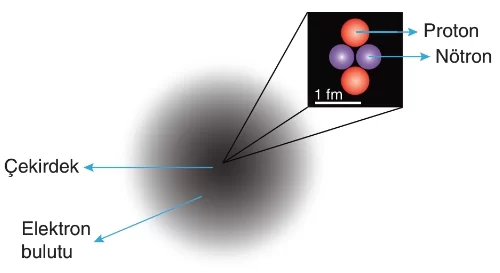
MODERN ATOM MODELİ
Heisenberg, yaptığı deneyler ve hesaplamalar sonucunda, elektronun hızının ve konumunun aynı anda yüksek doğrulukla belirlenemeyeceğini ortaya koymuştur. Bu duruma Belirsizlik İlkesi denir. Belirsizlik İlkesi’ne göre, Bohr atom modelinde bahsedildiği gibi elektronlar belirli dairesel yörüngelerde bulunamaz. Bunun yerine, elektronların çekirdek etrafında bulunma olasılığının yüksek olduğu hacimsel bölgeler tanımlanabilir.
- Çekirdeğe yakın bölgelerde elektronun bulunma olasılığı artarken, çekirdekten uzaklaştıkça bu olasılık azalır. Elektronun belirli bir bölgede bulunma olasılığı yoktur.
- Elektronların bulunma olasılıklarının en yüksek olduğu uzay bölgelerine orbital adı verilir.
Aşağıdaki grafik, hidrojen atomundaki elektronun çekirdekten belirli uzaklıklardaki bulunma olasılığını göstermektedir.
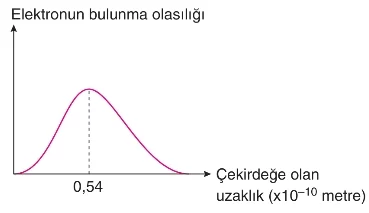
Grafiğe göre:
- Elektron, çekirdekten herhangi bir uzaklıkta bulunabilir.
- Elektronun çekirdekten belirli bir uzaklıkta bulunma olasılığı en yüksektir.
- Bohr atom modelindeki yörünge kavramı hatalıdır.
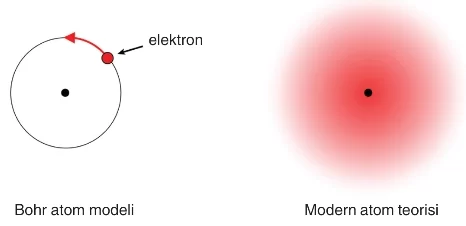
Bohr atom modeline göre elektronlar belirli yörüngelerde bulunur. Modern atom teorisine göre ise elektronlar orbitallerde bulunur.






